LOPL gydymas tiotropiu: apsaugokime pacientus nuo paūmėjimų pasekmių
Lėtinė obstrukcinė plaučių liga (LOPL) yra ypatingos socialinės, sveikatos priežiūros ir ekonominės svarbos liga, nes mirštamumo priežasčių skalėje užima 4 vietą po išeminės širdies ligos, piktybinių navikų ir smegenų kraujagyslių ligų (1). Be to, prognozuojama, kad 2020 metais ji bus trečia pagal dažnį mirties priežastis (2).
Nustatyta, kad mirštamumą nuo LOPL didina kai kurie svarbūs veiksniai: sumažėjęs forsuoto iškvėpimo tūris per 1 sek. (FEV1) (3, 4), vyresnis paciento amžius (4), hipoksemija (5), hiperkapnija (3), gretutinės ligos (3, 4, 6), plautinė hipertenzija (7) ir padidėjęs kūno masės indeksas (8), taip pat dusulys (9), pablogėjusi su sveikatos būkle susijusi gyvenimo kokybė (10) ir sumažėjęs fizinio krūvio toleravimas (11). Pastaraisiais metais daug dėmesio skiriama LOPL paūmėjimams, nes jie yra ne mažiau svarbus veiksnys, nulemiantis paciento prognozę, ypač sunkūs paūmėjimai, dėl kurių pacientą tenka gydyti stacionare (12).
LOPL paūmėjimų svarba
Natūraliai LOPL eigai būdingi paūmėjimai. Jais vadiname ūminius įvykius, kuriems būdinga LOPL simptomų pablogėjimas, palyginti su kasdieniu jų varijavimu, kurie reikalauja gydymokoregavimo (13). Paūmėjimui nustatyti paprastai vertinami LOPL simptomai: dusulys, kosulys, skrepliavimas, ankštumas krūtinėje ir švokštimas.
Paūmėjimų metu keičiasi LOPL būdinga pablogėjusi plaučių funkcija (14, 15), dėl kurios sumažėja fizinis aktyvumas (16), pablogėja gyvenimo kokybė (17) ir padidėja mirštamumo rizika (13). Dėl jų taip pat padidėja sveikatos priežiūros išlaidos (18), todėl dažniausiai klinikiniuose tyrimuose paūmėjimai laikomi svarbia išeitimi, o jų prevencija yra vienas pagrindinių LOPL gydymo tikslų (19).
Nustatyta, kad dėl paūmėjimo su hiperkapnija ir acidoze hospitalizuotų pacientų mirštamumas stacionare siekia 10 proc. (20), po išrašymo per 1 metus mirštamumas pasiekia 40 proc., o per 3 metus – net 49 proc. (20–24).
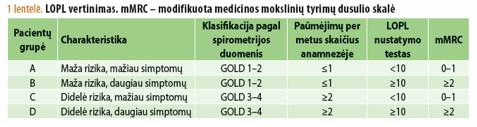
Pagal šių dienų rekomendacijas parenkant individualizuotą LOPL gydymą pacientui, atsižvelgiama ne vien į jo plaučių funkciją, bet ir į paūmėjimų skaičių anamnezėje (1 lentelė) (25). Nustatyta, kad jis yra svarbus prognostinis paūmėjimų ateityje rodiklis (26).
Ligai progresuojant, paūmėjimai dažnėja ir sunkėja, o vienintelis veiksnys, pagal kurį galima numatyti ateityje galinčių atsirasti paūmėjimų dažnį, taip pat polinkį jiems išsivystyti bei ligos sunkumą, yra anamnezėje buvę paūmėjimai, ypač tie, kuriuos reikėjo gydyti stacionare (25). Todėl pastarųjų metų LOPL gydymo rekomendacijose vienas pagrindinių LOPL gydymo tikslų – paūmėjimų prevencija (13).
Naujausios medikamentinio LOPL gydymo rekomendacijos
Pagal atnaujintas 2014 metų GOLD LOPL diagnostikos, gydymo ir prevencijos rekomendacijas, šia liga sergančiųjų pagrindiniai gydymo tikslai sugrupuoti į 2 grupes: mažinantys simptomų dažnį ir mažinantys riziką (13). Mažinantys simptomų dažnį tikslai: simptomų slopinimas, fizinio krūvio toleravimo gerinimas ir sveikatos būklės gerinimas. Mažinantys riziką tikslai – tai ligos progresavimo prevencija, paūmėjimų gydymas ir prevencija bei mirštamumo mažinimas (13).
Medikamentinis gydymas skiriamas individualiai kiekvienam pacientui, atsižvelgiant į tai, kuriai grupei jis priskiriamas (2 lentelė).
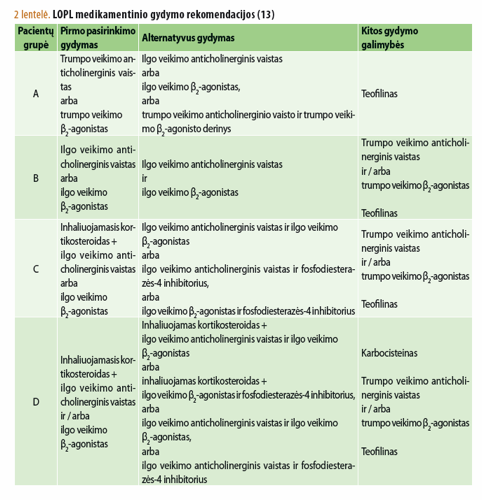
Būtina pabrėžti, kad renkantis vaistą ar vaistų derinį, svarbu atsižvelgti ir į jo formą: verčiau skirti ilgo, o ne trumpo veikimo tiek anticholinerginį vaistą, tiek β2-agonistą (įrodymų lygmuo A). Trumpo ir ilgo veikimo bronchus atpalaiduojančių preparatų (tiek anticholinerginių, tiek β2- agonistų) derinys gali būti skiriamas tik tiems pacientams, kuriems vieno vaisto nepakanka simptomams kontroliuoti (įrodymų lygmuo B). Be to, inhaliuojamieji bronchus atpalaiduojantys preparatai, atsižvelgiant į nepageidaujamus poveikius, gydymo metu pranašesni nei geriamieji (įrodymų lygmuo A).
Teofilinas nerekomenduojamas dėl mažo veiksmingumo ir daugybės nepageidaujamų poveikių, išskyrus tuos atvejus, kai pacientas negali dėl kurių nors priežasčių vartoti ilgo veikimo bronchus atpalaiduojančių vaistų (įrodymų lygmuo B).
Atkreiptinas dėmesys į tai, kad ilgo veikimo anticholinerginiai vaistai, kurių vienintelis atstovas tiotropis, rekomenduojami kaip pirmo pasirinkimo vaistai B, C ir D grupių LOPL sergantiems pacientams, o kaip antro pasirinkimo – visų LOPL sergantiems grupių pacientams (13).
Tiotropio Respimat® palyginimas su tiotropio HandiHaler®
Tiotropis – vienintelis ilgo veikimo inhaliuojamasis anticholinerginis preparatas, kuris pagerina plaučių funkciją, gyvenimo kokybę, fizinį pajėgumą ir sumažina paūmėjimus sergantiesiems LOPL (27–30). Daugelyje šalių šis vaistas tiekiamas sausų miltelių pavidalu (dozė 18 μg), įkvepiamų iš HandiHaler® prietaiso (31), ir vandeninio tirpalo pavidalu (dozė 5 μg), įkvepiamo iš Respimat® inhaliatoriaus (32). Respimat® ir HandiHaler® tiotropio poveikį palyginus 4 savaites trukusiame tyrime, paaiškėjo, kad jie labai panašūs veiksmingumu, saugumu ir farmakokinetika (33, 34), tačiau Respimat® veiksmingiau sumažino LOPL paūmėjimų (28, 30).
Vertinant Respimat® saugumą, atlikta 3 tyrimų, trukusių 1 metus, ir vieno 6 mėnesių trukmės placebu kontroliuojamo tyrimo post-hoc jungtinė analizė, kuri parodė, kad 5 μg tiotropio Respimat® buvo susijęs su didesniu, nei tikėtasi, per tyrimo laikotarpį mirštamumu (rizikos koeficientas (RK) 1,33; 95 proc. patikimumo intervalas (PI) 0,93– 1,92), daugiausia tarp širdies ritmo sutrikimų turinčių pacientų (32, 35). Tokie duomenys sukėlė daug diskusijų apie visų anticholinerginių vaistų, taip pat ir tiotropio Respimat®, saugumą, nes nebuvo galima paaiškinti priežasties (40).
Tyrime UPLIFT (angl. Understanding Potential Long-Term Impacts on Function with Tiotropium) lyginant HandiHaler® tiotropį su placebu nustatyta, kad vaisto grupėje mirštamumas buvo mažesnis (14,4 proc., palyginti su 16,3 proc., RK 0,87; 95 proc. PI 0,76–0,99) (30).
Be to, kai kurios metaanalizės neparodė tiotropio HandiHaler® ar Respimat® ir LOPL sergančiųjų mirštamumo tarpusavio ryšio (36, 41–43). Kadangi tiotropio Respimat® 5 μg ir tiotropio HandiHaler® 18 μg saugumo palyginimo tarpusavyje duomenų buvo mažai (6 448 pacientai ir 5 487 pacientų metai Respimat®, ir 17 014 pacientų bei 23 934 pacientų metai HandiHaler® grupėse), tiksliai nustatyti tiotropio Respimat® ir mirštamumo tarpusavio ryšį nebuvo galima (35).
Tuo tikslu atliktas tyrimas TIOSPIR (angl. Tiotropium Safety and Performance in Respimat) (39). Tai atsitiktinės imties, dvigubai aklas, paralelinių grupių tyrimas, kuriame vertintas 2,5 μg ar 5 μg tiotropio Respimat®, vartojamo 1 k./d., palyginti su 18 μg tiotropio HandiHaler®, vartojamo 1 k./d., saugumas ir veiksmingumas. Tyrime dalyvavo 20 313 pacientų. Iš jų 17 135 suvartojo bent vieną tiriamojo vaisto dozę. Kiekvienas tiriamųjų vartojo arba Respimat®, arba HandiHaler® inhaliatorių, taip pat placebo inhaliatorių. Taigi pacientai vartojo tiotropio Respimat® 2,5 μg (2 inhaliacijos po 1,25 μg) ar 5 μg (2 inhaliacijos po 2,5 μg), arba 18 μg tiotropio HandiHaler® ir kartu placebo.
Pacientai stebėti 12 savaičių, paskutinis vizitas – praėjus 30 dienų po gydymo. Iš tyrime dalyvavusių gydytų pacientų 13 199 (77,1 proc.), nenutraukė gydymo anksčiau laiko. Visose 3 tiriamųjų grupėse nutraukusiųjų gydymą skaičius buvo panašus, dauguma gydymą nutraukė dėl nepageidaujamojo vaistų poveikio.
Iš viso 90 proc. pacientų gydymą baigė, o tyrimo metu suvartojo 80–120 proc. tiriamų vaistų dozių. Vidutinė gydymo trukmė siekė 835 dienas visose 3 tiriamųjų grupėse, stebint vidutiniškai 2,3 metų. Tiriamojo vaisto veikimo ekspozicija siekė 11 405 paciento metų vartojusiųjų 2,5 μg tiotropio Respimat®, 11 343 paciento metus 5 μg Respimat® ir 11 337 paciento metus 18 μg HandiHaler® grupėse.
Pacientų charakteristikos tarp grupių reikšmingai nesiskyrė. Vidutinis tiriamųjų amžius buvo 65±9 metai, 71 proc. sudarė vyrai, iš kurių 38 proc. teberūkė tyrimo metu, o vidutinis FEV1 buvo 48 proc. numatyto dydžio. Gydymo pradžioje apie 50 proc. pacientų vartojo širdies ir kraujagyslių sistemos ligoms gydyti skirtų medikamentų, taip pat ilgo veikimo ß2 agonistų (62 proc. vartojo iki tyrimo, o 68 proc. – tyrimo metu), gliukokortikoidų (59 proc. vartojo iki tyrimo, 68 proc. – tyrimo metu). Apie 11 proc. tiriamųjų anamnezėje buvo aritmijų.
Pirmine tyrimo išeitimi laikyta mirtis dėl bet kokios priežasties. Šios išeities (bendrojo mirštamumo) rizikos santykis 5 μg Respimat® grupėje buvo 0,96, palyginti su HandiHaler® grupe (95 proc. PI 0,84–1,09), o 2,5 μg Respimat® grupėje 1,00, palyginti su HandiHaler® grupe (95 proc. PI 0,87–1,14). Kadangi PI viršutinė riba gerokai nesiekė iš anksto prognozuotos 1,25 vertės, abi tiotropio Respimat® dozės prilygo tiotropiui HandiHaler® pagal bendrojo mirštamumo riziką.
Mirtis dėl bet kokios priežasties ištiko 7,7 proc. pacientų 2,5 μg tiotropio Respimat®, 7,4 proc. 5 μg tiotropio Respimat® ir 7,7 proc.
18 μg tiotropio HandiHaler® grupėse. Panašūs rezultatai gauti ir analizuojant pacientų, gavusių bent vieną vaisto dozę, duomenis (atitinkamai 6,3 proc., 5,7 proc. ir 6,3 proc.). Mirties priežasčių pasiskirstymas tarp grupių buvo panašus, įskaitant ir mirties dėl širdies ir kraujagyslių ligų dažnį (atitinkamai 2,1 proc., 2,0 proc. ir 1,8 proc.). Statistiškai reikšmingų skirtumų tarp abiejų dozių tiotropio Respimat® ir tiotropio HandiHaler® grupių neužfiksuota.
Taip pat padidėjusios mirštamumo rizikos nenustatyta ir tiems pacientams (n=1 221), kurie anamnezėje sirgo širdies aritmijomis (bendrasis mirštamumas 5 μg tiotropio Respimat® grupėje 10,6 proc., o 18 μg tiotropio HandiHaler® – 12,9 proc.; RS 0,81, 95 proc. PI 0,58–1,12).
Kita pirmine išeitimi laikyta pirmojo LOPL paūmėjimo rizika. Lyginant LOPL paūmėjimų dažnį 5 μg tiotropio Respimat® ir 18 μg HandiHaler® grupėse, nustatytas RS 0,98 (95 proc. PI 0,93–1,03) (3 lentelė ir 1A bei 1B pav.), o skirtumas buvo statistiškai nereikšmingas (p=0,42).
Analogiškas rezultatas gautas lyginant 2,5 μg tiotropio Respimat® ir 18 μg HandiHaler® grupes (p=0,56). Pacientų, kuriems LOPL paūmėjo 5 μg Respimat® grupėje, buvo 47,9 proc., o HandiHaler® grupėje – 48,9 proc. Iki LOPL paūmėjimo praėjo vidutiniškai atitinkamai 756 ir 719 dienų. Visose trijose grupėse vidutinio sunkumo ir sunkių LOPL paūmėjimų dažnis buvo panašus ir statistiškai reikšmingai tarp grupių nesiskyrė.

Sunkių nepageidaujamų poveikių užfiksuota trečdaliui tiriamųjų. Kaip ir tikėtasi, daugiausia buvo kvėpavimo takų sutrikimų (17,8 proc. 2,5 μg Respimat®, 16,8 proc. 5 μg Respimat® ir 17,0 proc. HandiHaler® grupėse). Nepageidaujamų širdies ir kraujagyslių įvykių visose tiriamųjų grupėse pasireiškė panašiai: atitinkamai 3,9 proc., 3,9 proc. ir 3,6 proc. Aritmijų dažnis buvo atitinkamai 2,3 proc., 2,1 proc. ir 2,1 proc. Taigi, ištyrus daugiau nei 17 tūkst. pacientų, sergančių LOPL, galima teigti, kad tiotropio dozės, esančios skirtingų tipų inhaliatoriuose, yra panašiai saugios ir veiksmingos, todėl gali būti užtikrintai skiriamos LOPL gydyti.
Apibendrinimas
Atnaujintose 2014 metų GOLD LOPL gydymo gairėse daug dėmesio skiriama sergančių pacientų LOPL paūmėjimų prevencijai ir gydymui, ypač sunkių, kuriuos reikia gydyti stacionare. Įrodyta, kad jie turi įtakos ateityje galimų paūmėjimų dažniui, taip pat LOPL sunkumui, pacientų gyvenimo kokybei, be to, didina mirštamumo riziką (13).
Parenkant individualiai kiekvienam pacientui gydymą, remiamasi ne tik spirometrijos duomenimis, bet ir anamnezėje buvusiais paūmėjimais (1 lentelė). Renkantis, kokį vaistą skirti, gydytojui paliekamas gana platus pasirinkimas, atsižvelgiant į paciento galimybes ir poreikius. Beveik visų grupių pacientams kaip pirmo pasirinkimo ir visų grupių pacientams kaip antro pasirinkimo vaistas gali būti skiriamas ilgo veikimo anticholinerginis vaistas tiotropis, kuris veiksmingai sumažina LOPL paūmėjimų dažnį (39).
Rinkoje yra 2 tiotropio inhaliatorių formos: Respimat® (5 μg/d. dozė) ir HandiHaler® (18 μg/d. dozė). Lyginant abi formas, paūmėjimų dažnio, mirštamumo ir saugumo skirtumų nenustatyta, net ir širdies bei kraujagyslių ligomis sergantiems pacientams (39), todėl tai puikus pasirinkimas LOPL sergantiems pacientams gydyti.
Parengė gyd. Liucija Vaitkevičiūtė

