C1 esterazės inhibitoriaus stokos sukelta angioedema
Simona Abraitytė
Įvadas
C1 esterazės inhibitoriaus (C1-INH) stoka yra reta imuninės sistemos patologija, kuria sergant dėl bradikinino pertekliaus išprovokuojami spontaniniai angioedemos priepuoliai. Jie sukelia pacientui didelį diskomfortą, psichoemocinius sutrikimus, blogina gyvenimo kokybę ir gali kelti grėsmę gyvybei. Bradikinino indukuotos angioedemos yra retas, dažniausiai autosominiu dominantiniu būdu paveldimas susirgimas. Angioedema yra dažnas simptomas klinikinėje praktikoje, su kuriuo gali susidurti bet kuris gydytojas. Vadinasi labai svarbu mokėti atpažinti ir diferencijuoti šio klinikinio požymio kilmę.
Angioedema – tai staigus gilesnių odos sluoksnių ir poodžio paburkimas (1). Šis simptomas, sergant dilgėline, gali pasireikšti kartu su bėrimu pūkšlėmis. Tokiu atveju angioedemą sukelia histamino išsiskyrimas (2). Angioedema gali išsivystyti ir esant komplemento komponentų kiekybiniam ar kokybiniam funkcijos sutrikimui. Tokiu atveju angioedema diagnozuojama kaip atskira liga (2).
Komplemento sistemos reguliacinis baltymas C1-INH – tai fermentas, kuris reguliuoja bradikinino kiekį organizme (3). Šio fermento stoka sukelia angioedemą, nes sutrikdo kalikreino ir kinino sistemos reguliaciją ir dėl to gaminama gerokai daugiau bradikinino (4). C1-INH stoka gali būti tiek įgimta, tiek įgyta (4). Paveldima C1-INH stokos išprovokuota angioedema serga 1 iš 50 tūkst. žmonių, įgyta C1-INH stokos sukelta angioedema sergama dar rečiau – 1 iš 600 tūkst. žmonių pasaulyje (5).
Šio straipsnio tikslas apžvelgti C1-INH stokos sukeltos angioedemos patogenezę, diagnostiką, diferencinę diagnostiką ir gydymo principus.
Klinikinė išraiška ir diferencinė diagnostika
Angioedema mokslinėje literatūroje gali būti vadinama Kvinkės edema, angioneurotine edema, didžiąja dilgėline (angl. giant hives) (6). Angioedemos metu pokyčiai vyksta odos giliuosiuose sluoksniuose ir poodyje. Kliniškai tai pasireiškia asimetrišku tam tikros kūno vietos paburkimu ir patinimu. Vienas dažnų lydinčių ir pacientus varginančių simptomų yra skausmas. Oda tinimo vietoje būna nepakitusi arba gali pasireikšti neaiškių ribų paraudimas. Tinimas išlieka iki 72 val. ar net ilgiau (3).
Angioedema gali pasireikšti bet kurioje kūno vietoje – lūpose, liežuvyje, veide, galūnėse, žarnyne (6). Kiekvieno angioedemos priepuolio metu paburkimas ir patinimas gali būti vis kitoje vietoje. Veido angioedema gali sukelti diskomfortą ir sutrikdyti kasdienę veiklą bei socialinį gyvenimą (6). Gerklų angioedema yra ūmi ir gyvybei grėsmę kelianti būklė. Negydoma gerklų angioedema sukelia mirtį apie 25–40 proc. pacientų (7). 50 proc. visų pacientų, turinčių C1-INH stoką, gerklų angioedemos priepuolis gali pasireikšti bent kartą gyvenime (7, 8). Angioedema gali pasireikšti ir vidaus organuose, pavyzdžiui, žarnų sienelėse. Tai sukelia pilvo skausmą, pykinimą, vėmimą, viduriavimą, bendrą silpnumą – visi šie simptomai yra priskiriami ūmaus pilvo sindromui, kurio dažniausia priežastis būna apendicitas. Laiku atpažinus C1-INH stokos sukeltą angioedemą galima skirti tinkamą gydymą ir išvengti nereikalingos chirurginės intervencijos. Vieno klinikinio tyrimo metu paaiškėjo, kad pacientams, kuriems nustatytas C1-INH stoka, dažnai atliekamos nereikalingos chirurginės intervencijos (7–9). Skyrus tinkamą gydymą, galima išvengti ar sumažinti spontaninių angioedemų dažnį (5, 7).
Angioedema diagnozuojama remiantis paciento anamneze ir objektyvia apžiūra. Angioedema turėtų būti diferencijuojama nuo anasarkos (tai išplitęs minkštųjų audinių pabrinkimas, kuris yra simetriškas, ir šis klinikinis požymis yra kitų ligų, pavyzdžiui, inkstų, miksedemos, pseudoangioedemos (pvz., vena cava superior suspaudimo sindromas), Melkerssono-Rosenthalo sindromo (veidinio nervo neuropatija, kuri kliniškai gali pasireikšti veido ar lūpų tinimu) sukeltas padarinys (2).
C1-INH stokos sukelta angioedema gerokai retesnė ir yra atspari gydymui antihistamininiais vaistais, sisteminiais gliukokortikoidais bei adrenalinu (2, 7).
Įtariant C1-INH stokos sukeltą angioedemą, rekomenduojama atlikti komplemento 4 komponento (C4) kiekio tyrimą. C4 sumažėja net remisijos metu ir tik 5 proc. visų sergančiųjų išlieka nepakitęs ar padidėjęs (7). Diagnozę patvirtina C1-INH aktyvumo (funkcijos) ir kiekio tyrimas (10). Taip pat atliekamas antikūnų prieš C1-INH tyrimas (5). Sergant paveldima angioedema, C1-INH antikūnų titras yra normalus, o įgytos angioedemos atveju sumažėja 70 proc. pacientų (5). C1-INH stokos diagnostikos algoritmas pateiktas 1 pav.
1 pav. C1-INH stokos diagnostikos algortimas (10)
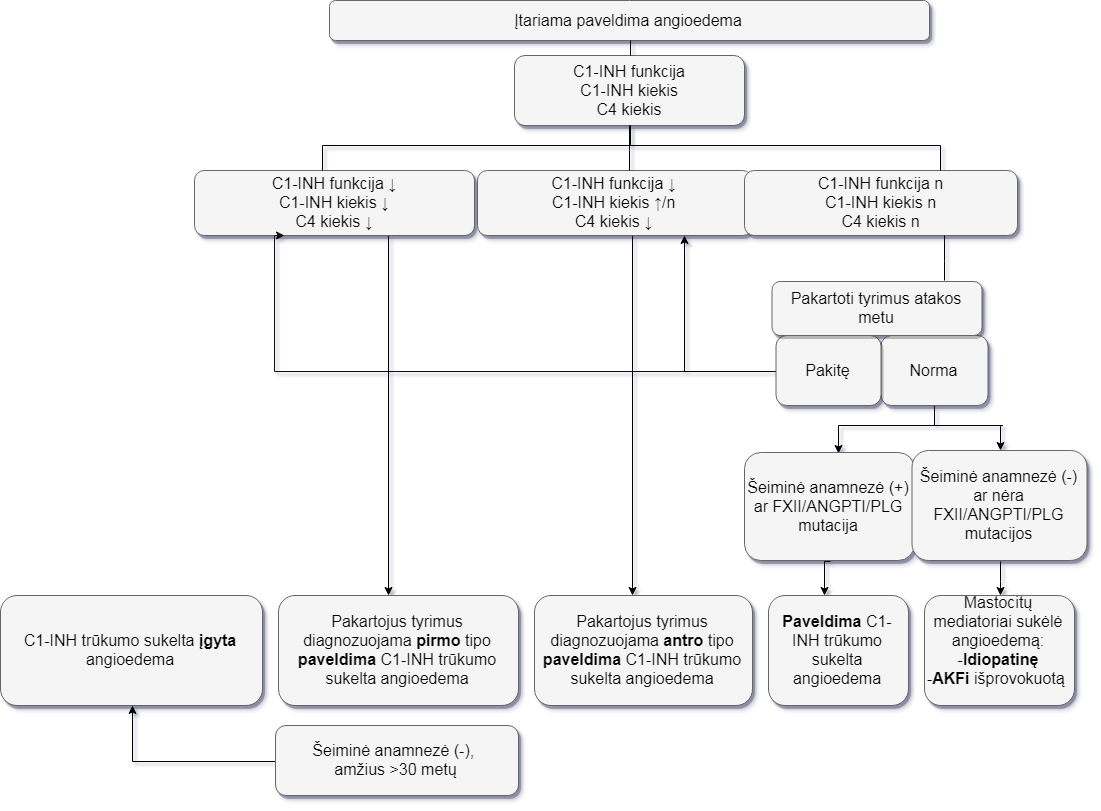
*n – normali.
C1-INH reikšmė ir C1-INH stokos sukeltos angioedemos patogenezė
C1-INH tiesiogiai susijęs su kalikreino ir kinino sistema bei uždegiminio mediatoriaus bradikinino reguliacija. Šio fermento stoka sukelia kalikreino ir kinino kelio sutrikimus ir perteklinę bradikinino gamybą (7–9).
C1-INH stokos sukelta angioedema skirstoma į keturis tipus, kurių pagrindiniai skirtumai pateikiami 1 lentelėje. C1-INH yra serpinų šeimos atstovas – serino proteazių inhibitorius. C1-INH genas yra 11 chromosomoje ir yra vadinamas SERPING1. Būtent šio geno mutacijos sukelia C1-INH stoką. Jei yra randama šio geno mutacija, angioedema yra priskiriama pirmam tipui, t. y. autosominiu dominantiniu būdu paveldimai angioedemai. Apie 75 proc. pacientų, turinčių šią mutaciją, nurodo, kad šios ligos atvejų yra šeimoje, tačiau apie 25 proc. visų ligos atvejų nustatoma de novo mutacija (2, 11).
Trečio angioedemos tipo atveju endogeninis C1-INH slopina proteazes ir faktorius (pvz., XII ir XIIa), dalyvaujančius fiziologinėse komplemento bei kalikreino ir kinino sistemų kaskadose. Šios sistemos dalyvauja tokiuose procesuose kaip koaguliacija ir fibrinolizė. XII faktorius yra autoaktyvinamas generuoti XIIa faktorių, kuris skaldo prekalikreiną, o šis generuoja plazmos kalikreiną. Plazmos kalikreinas aktyvina XII faktorių, kuris vėl generuoja XIIa faktorių ir skaldo stambiamolekulinį kininogeną, išlaisvinantį bradikininą. Uždegiminis mediatorius bradikininas susijungia su B2 receptoriais, kurie yra ant ląstelės paviršiaus, ir sudaro kompleksą. Šis kompleksas sukelia vazodilataciją, padidina kraujagyslių endotelio pralaidumą. Visa šių procesų kaskada sukelia angioedemą (7–9, 11).
Ne visais atvejais nustatomas sumažėjęs C1-INH kiekis. Šio fermento kiekis gali būti pakankamas, tačiau funkcija gali būti sutrikusi (9). Tokia patogenezė būdinga tiek įgimtai, tiek įgytai angioedemai (2, 5).
1 lentelė. C1-INH stokos sukeltos angioedemos tipai (2, 5, 7–12)
| Pirmas tipas | Antras tipas | Trečias tipas | Ketvirtas tipas |
| Įgimta | Įgimta | Įgimta | Įgyta |
| C1-INH ir C4 ↓, C1q – norma | C1-INH ir C4, C1q kiekiai – norma | C1-INH ir C4, C1q kiekiai – norma | C1-INH ir C4, C1q kiekiai ↓ |
| C1-INH funkcija nesutrikusi | C1-INH funkcija sutrikusi arba normali | C1-INH funkcija nesutrikusi | C1-INH funkcija sutrikusi |
| Vyrai ir moterys – 1:1 | Vyrai ir moterys – 1:1 | Vyrai < moterys | Vyrai ir moterys – 1:1 |
| 85 proc. visų C1-INH stokos atvejų | 15 proc. visų C1-INH stokos atvejų | Rečiausiai sutinkamas tipas | Labai retas |
| Serga jaunesni nei 20 metų pacientai | Serga jaunesni nei 20 metų pacientai | Serga vyresnės nei 40 metų moterys | Serga vyresni nei 40 metų pacientai |
| Mutacija 11 chromosomoje (SERPING1)*. Paveldima autosominiu dominantiniu būdu. 75 proc. šeiminė anamnezė (+), 25 proc. – de novo mutacija | Taškinė mutacija | Mutacijos ANGPT1* ar PLG* genuose | Gali išprovokuoti gretutinės ligos – hematologinės ar autoimuninės kilmės. Nėra šeiminės anamnezės |
*SERPING1 – angl. Serpin Peptidase Inhibitor Clade G Member 1, ANGPT1 – angioproteinas 1, PLG – plazminogenas.
C1-INH stokos sukeltos angioedemos gydymo principai
Siekiant išvengti angioedemos priepuolių, rekomenduojama vengti provokacinio veiksnio, kuris gali būti stresas, trauma, geriamiieji kontraceptikai (5). Vis dėlto dažnai pagrindinis angioedemą provokuojantis veiksnys yra nežinomas, ir angioedema pasireiškia spontaniškai (13).
C1-INH stokos sukelta angioedema nėra susijusi su dilgėline ar kita alergine liga, kurių metu vienas pagrindinių patogenezinių veiksnių yra histaminas. Todėl bradikinino indukuotos angioedemos gydymas antihistamininiais vaistais, gliukokortikoidais ar / ir adrenalinu nėra efektyvus (7). C1-INH stokos sukeltai angioedemai gydyti gali būti skiriamas simptominis arba profilaktinis gydymas.
Simptominis gydymas – tai vaisto skyrimas angioedemos priepuolio metu. Pagrindiniai medikamentai, kurie vartojami įgytos bei įgimtos ūmios angioedemos priepuolio metu, yra C1-IHN koncentratas, B2 receptorių antagonistas ikatibantas ir kalikreino inhibitorius ekalantidas (11). Jei nėra galimybės skirti šių vaistų, galimas gydymas tirpių detergentų paveikta plazma (angl. solvent detergent treated plasma – SDP) arba šviežiai šaldyta plazma (10).
Profilaktinis gydymas – tai vaistų skyrimas, siekiant išvengti angioedemos priepuolio. Jis gali būti trumpalaikis arba ilgalaikis. Ilgalaikio profilaktinio gydymo tikslas – sumažinti spontaninių angioedemų priepuolių dažnį ir simptomų sunkumą. Ilgalaikis profilaktinis gydymas laikomas efektyviu, kai angioedemų dažnis sumažėja daugiau nei 50 proc. (5). Trumpalaikio profilaktinio gydymo tikslas – išvengti angioedemos per planuojamą procedūrą ar intervenciją, pavyzdžiui, odontologinės kilmės intervenciją (4, 8).
Medikamentai, skiriami C1-INH stokos sukeltai angioedemai gydyti
Simptominiam ir profilaktiniam gydymui naudojamas C1-INH plazmos derivatas, kuris padidina C1-INH koncentraciją plazmoje. Susintetintas žmogaus C1-INH koncentratas angioedemai gydyti naudojamas jau nuo 1970 metų (9). Šiuo metu yra skiriami ir sintetiniai C1-INH koncentratai. Mokslinis tyrimas parodė, kad vartojant C1-INH plazmos derivatą po 1 000 VV 2 k./sav., spontaninės angioedemos priepuolių dažnis sumažėjo 50 proc., palyginti su placebu (14).
Sintetiniai androgenai – danazolas ir stanozolas – yra naudojami tiek trumpalaikio, tiek ilgalaikio profilaktinio gydymo metu. Dvigubai aklo, placebu kontroliuojamo tyrimo rezultatai parodė, kad androgenai sumažina angioedemos sunkumą bei dažnį (4). Tiesa, šis gydymas yra susijęs su nepageidaujamų reiškinių rizika. Dažniausi nepageidaujami reiškiniai, kuriuos sukelia androgenai, yra padidėję plaukuotumas, svoris, kraujospūdis, kepenų fermentų aktyvumas ir pakitęs balsas (15).
Angioedem taip pat gydoma ekalantidu. Tai rekombinantinis baltymas, sudarytas iš 60 aminorūgščių, tiesioginis kalikreino inhibitorius. Moksliniai tyrimai parodė, kad jis sumažina angioedemos trukmę, tačiau apie 5 proc. visų tiriamųjų pasireiškė alerginių reakcijų (4). Ekalantidas tinkamiausias ūmios angioedemos priepuoliui gydyti (16).
Dar vienas vaistas, skiriamas angioedemai gydyti, yra B2 receptorių antagonistas ikatibantas. Jis yra gerai toleruojamas. Naujausiuose klinikiniuose tyrimuose ikatibantas apie 80 proc. visų pacientų nesukėlė nepageidaujamų reiškinių (13). Įrodyta, kad ikatibantas yra efektyvus gydant pirmo ir antro tipo angioedemą bei AKFI sukeltą angioedemą (17).
Naujausias efektyvus gydymas yra biologinė terapija lanadelumabu (18). Tai monokloninis antikūnas, kuris sujungia aktyvų plazmoje esantį kalikreiną. Atliktuose klinikiniuose tyrimuose lanadelumabas buvo ne tik efektyvus ilgalaikiam profilaktiniam gydymui, bet ir sukėlė mažai nepageidaujamų reiškinių (18). Gydant paveldimą angioedemą, šis vaistas buvo efektyvesnis už placebą (8).
C1-INH stokos sukeltos angioedemos gydymas apibendrintas 2 lentelėje (18).
2 lentelė. C1-INH stokos sukeltos angioedemos gydymas (4, 5, 8, 13–22)
| Ūmi būklė – angioedemos priepuolio metu | Trumpalaikė profilaktika | Ilgalaikė profilaktika |
| Vengti provokacinių veiksnių: stresas, įtampa, geriamieji kontraceptikai ir kt. | ||
| C1-INH plazmos derivato infuzija i/v (žmogaus ar rekombinantinis preparatas) | Tikslas – išvengti angioedemos per planuojamą procedūrą ar intervenciją | Tikslas – sumažinti spontaninės angioedemos priepuolių dažnį ir simptomų sunkumą |
| Ikatibanto injekcija po oda (bradikinino B2 receptorių antagonistas) | C1-INH plazmos derivato infuzija | C1-INH plazmos derivato infuzija |
| Ekalantido injekcija po oda (plazmos kalikreino inhibitorius, kuris neleidžia kininogenui virsti bradikininu) | Testosterono preparatai: danozolas, stanozolas | Testosterono preparatai: danozolas, stanozolas |
| Intubacija, tracheostomija | Ikatibantas | Ikatibantas |
Apibendrinimas
C1-INH stokos sukelta angioedema yra reta patologija. Ji gali būti tiek įgimta, tiek įgyta. Angioedema gali pasireikšti bet kurioje kūno vietoje. Gerklų angioedema yra dažna ir gyvybei grėsminga būklė. C1-INH stokos sukelta angioedema diagnozuojama nustačius šio komplemento sistemos komponento stoką ar funkcijos nepakankamumą. Pirmojo pasirinkimo vaistas gydymui yra C1-INH koncentratas. Jis gali būti skiriamas ūmaus angioedemos priepuolio metu arba ilgalaikei ir trumpalaikei profilaktikai.
Leidinys „Internistas” Nr. 4 2020 m.
LITERATŪRA
1. Busse PJ, Smith T. (2017). Histaminergic Angioedema. Immunology and Allergy Clinics of North America, 37(3), 467–481.
2. LoVerde D, Files DC, Krishnaswamy G. (2017). Angioedema. Critical Care Medicine, 45(4), 725–735.
3. Riedl MA, Grivcheva-Panovska V, Moldovan D, et al. (2017). Recombinant human C1 esterase inhibitor for prophylaxis of hereditary angio-oedema: a phase 2, multicentre, randomised, double-blind, placebo-controlled crossover trial. The Lancet, 390(10102), 1595–1602.
4. Zeerleder S, Levi M. (2016). Hereditary and acquired C1-inhibitor-dependent angioedema: from pathophysiology to treatment. Annals of Medicine, 48(4), 256–267.
5. Zanichelli A, Azin GM, Wu MA, et al. (2017). Diagnosis, Course, and Management of Angioedema in Patients With Acquired C1-Inhibitor Deficiency. The Journal of Allergy and Clinical Immunology: In Practice, 5(5), 1307–1313.
6. Radonjic-Hoesli S, Hofmeier KS, Micaletto S, et al. (2017). Urticaria and Angioedema: an Update on Classification and Pathogenesis. Clinical Reviews in Allergy & Immunology, 54(1), 88–101.
7. Fragnan NTML, et al. (2018). Hereditary angioedema with C1 inhibitor (C1-INH) deficit: the strength of recognition (51 cases). Brazilian Journal of Medical and Biological Research, 51(12).
8. Busse PJ, et al. (2018). Lanadelumab for the Prophylactic Treatment of Hereditary Angioedema with C1 Inhibitor Deficiency: A Review of Preclinical and Phase I Studies. BioDrugs. 33(1), 33-43.
9. Horiuchi T. (2019). Hereditary Angioedema from 1888 to 2018 -Progress and Problems. Internal Medicine. 57(21), 3065-3066.
10. Cicardi M, et al. HAWK under the patronage of EAACI (European Academy of Allergy and Clinical Immunology). (2014). Classification, diagnosis, and approach to treatment for angioedema: consensus report from the Hereditary Angioedema International Working Group. Allergy. 69(5):602-16.
11. Morelli C, et al. (2018). Chemotherapy in Patients with Hereditary Angioedema. Anticancer Research, 38(12), 6801–6807.
12. Otani IM, Banerji A. (2017). Acquired C1 Inhibitor Deficiency. Immunology and Allergy Clinics of North America, 37(3), 497–511.
13. Zanichelli A, et al. (2017). Long-term safety of icatibant treatment of patients with angioedema in real-world clinical practice. Allergy, 72(6), 994–998.
14. Dempster J. (2018). Practicalities of a reduced volume formulation of a C1-INH concentrate for the treatment of hereditary angioedema: real-life experience. Allergy, Asthma & Clinical Immunology, 14(1).
15. Leru PM, et al. (2018). Nine year follow-up of a rare case of angioedema due to acquired C1-inhibitor deficiency with late onset and good response to attenuated androgen. Allergy, Asthma & Clinical Immunology, 14(1).
16. Firszt R, Duffey H. (2015). Management of acute attacks of hereditary angioedema: role of ecallantide. Journal of Blood Medicine, 115.
17. Sinert R, et al. (2017). Randomized Trial of Icatibant for Angiotensin-Converting Enzyme Inhibitor–Induced Upper Airway Angioedema. The Journal of Allergy and Clinical Immunology: In Practice, 5(5), 1402–1409.e3.
18. Banerji A, et al. (2018). Effect of Lanadelumab Compared With Placebo on Prevention of Hereditary Angioedema Attacks. JAMA, 320(20), 2108.
19. Didier G. Ebo, et al. Hereditary Angioedema in Childhood: An approach to management. Pediatic Drugs 2010; 12 (4): 257-268.
20. Lewis LM, et al. (2015). Ecallantide for the Acute Treatment of Angiotensin-Converting Enzyme Inhibitor–Induced Angioedema: A Multicenter, Randomized, Controlled Trial. Annals of Emergency Medicine, 65(2), 204–213.
21. Amann T, et al. (2019). Glyco-engineered CHO cell lines producing alpha-1-antitrypsin and C1 esterase inhibitor with fully humanized N-glycosylation profiles. Metabolic Engineering. 52, 143-152.
22. Valerieva A, et al. (2018). Recombinant human C1 esterase inhibitor (Conestat alfa) for prophylaxis to prevent attacks in adult and adolescent patients with hereditary angioedema. Expert Review of Clinical Immunology. 14(9), 707-718.

